期刊导读:于聚乙二醇干扰素α(PEGIFNα)是慢乙肝患者临床治愈和远期获益的最佳选择
编者按:慢乙肝治疗的最终目标是降低肝硬化、肝癌等远期不良结局发生风险。自2016年起,已有多项研究发现干扰素α(IFNα)类药物预防慢乙肝患者肝癌发生风险显著优于核苷类药物(NAs)(相关链接一、二、三、四、五),因此,目前基于聚乙二醇干扰素α(PEGIFNα)是慢乙肝患者追求临床治愈和远期获益的最佳选择。
近期,来自厦门市中医院的毛乾国教授、梁惠卿教授团队发表的最新研究结果显示:不论患者是否有代偿期肝硬化,基于IFNα的治疗在降低慢乙肝患者远期不良结局风险(失代偿肝硬化、肝衰竭、肝癌、肝移植及死亡)方面显著优于NAs,且在肝癌高风险人群中,IFNα预防肝癌发生风险也显著优于NAs。

研究方法
这是一项回顾性队列研究,研究对象为2004年5月至2017年12月在厦门市中医院肝病中心接受常规抗病毒药物治疗的慢乙肝患者。收集的数据包括家族史、年龄、性别、肝硬化状态、抗病毒药物、常规血液生化和病毒学检查、肝脏成像结果、磁共振成像和组织学结果等。所有数据均收集自纳入患者的就诊之日。研究包括初治患者和经治患者,患者均进行了长期的规律随访。主要疗效指标为不良结局(失代偿肝硬化、肝衰竭、肝癌、肝移植和死亡)发生率。
IFNα治疗组包括(1)单药治疗:普通IFNα,PEGIFNα;(2)IFNα序贯或联合NAs治疗。患者使用IFNα治疗时间至少为24周。
NAs治疗组包括(1)单药治疗:ETV,TDF,LdT,ADV,LAM;(2)使用不同NAs序贯或联合。
患者特征
研究共筛选1332例患者,最终1247例患者纳入分析。其中NAs组370例,IFNα组877例。中位随访时间为5.2年(IQR4.5-6.0)。对两组患者基线特征进行比较发现IFNα组患者年龄、代偿期肝硬化比例、AFP水平和总胆红素水平低于NAs组,但HBeAg阳性比例、血小板计数、白蛋白、HBVDNA水平高于NAs。所有患者均有肝活检数据。IFNα和NAs组分别有41例和65例代偿期肝硬化患者。经过倾向性评分匹配(PSM)后,两组各301例患者,基线特征均无显著差异。
全队列PSM前后的基线特征
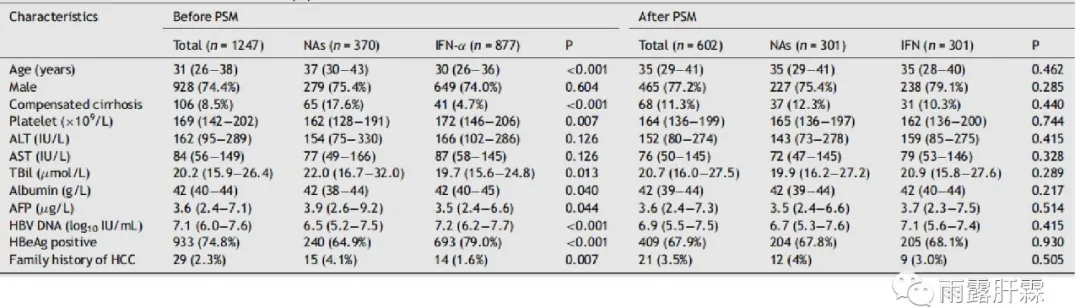
为了消除既往抗病毒治疗对远期结局的影响,也对初治队列进行了分析。共有1146例初治患者,中位随访5.3年(IQR4.5-6.1),其中IFNα组806例,NAs组340例。通过PSM后,两组各276例,各基线指标无显著性差异。
初治队列PSM前后的基线特征
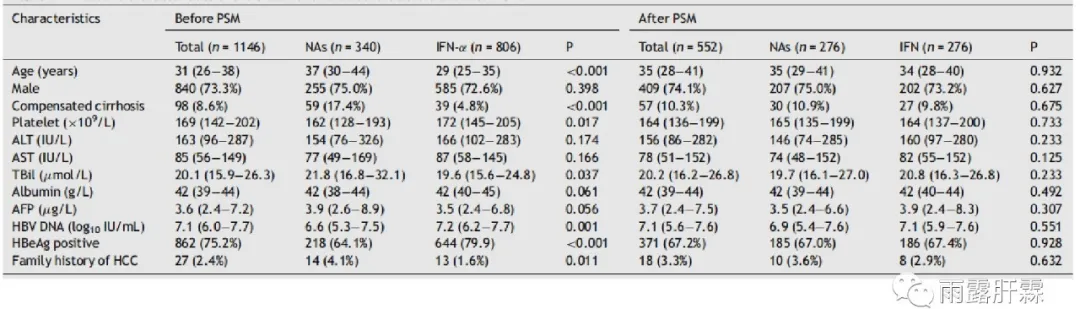
研究结果
01 全队列PSM前后,IFNα组的不良结局发生风险均显著低于NAs组
随访期间,共有26例患者发生了不良结局,其中NAs组20例,IFNα组6例。IFNα组总的累积不良结局发生率显著低于NAs组(2.3%vs.13.9%,P<0.001)。IFNα组3、5、7、10年的累积不良结局发生率分别为0.1%、0.6%、0.6%和1.1%。而NAs组3、5、7、10年的累积不良结局发生率分别为2.2%、3.8%、9.9%和11.9%。另外,不论是对于非肝硬化和肝硬化患者,IFNα组的累积不良结局发生风险均显著低于NAs组(P=0.002,P=0.045)。
PSM后,IFNα组的累积不良结局发生率仍显著低于NAs组(0.3%vs.10.0%,P=0.002)。IFNα组3、5、7、10年的累积不良结局发生率分别为0.3%、0.3%、0.3%和0.3%。而NAs组3、5、7、10年的累积不良结局发生率分别为1.7%、2.6%、7.1%和10.0%。
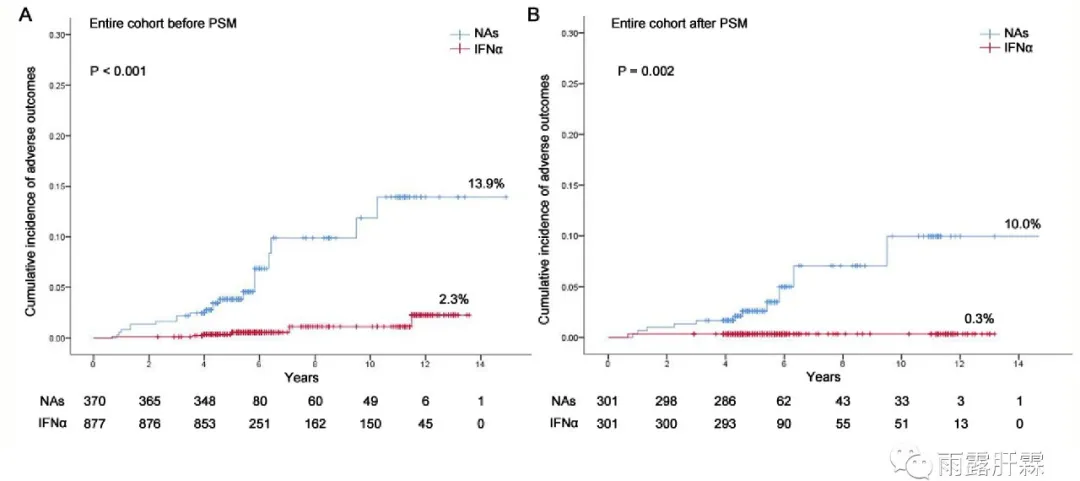
全队列IFNα组和NAs组PSM前后的累积不良结局发生率
02 全队列PSM前后,基于IFNα的治疗均与降低不良结局发生风险独立相关
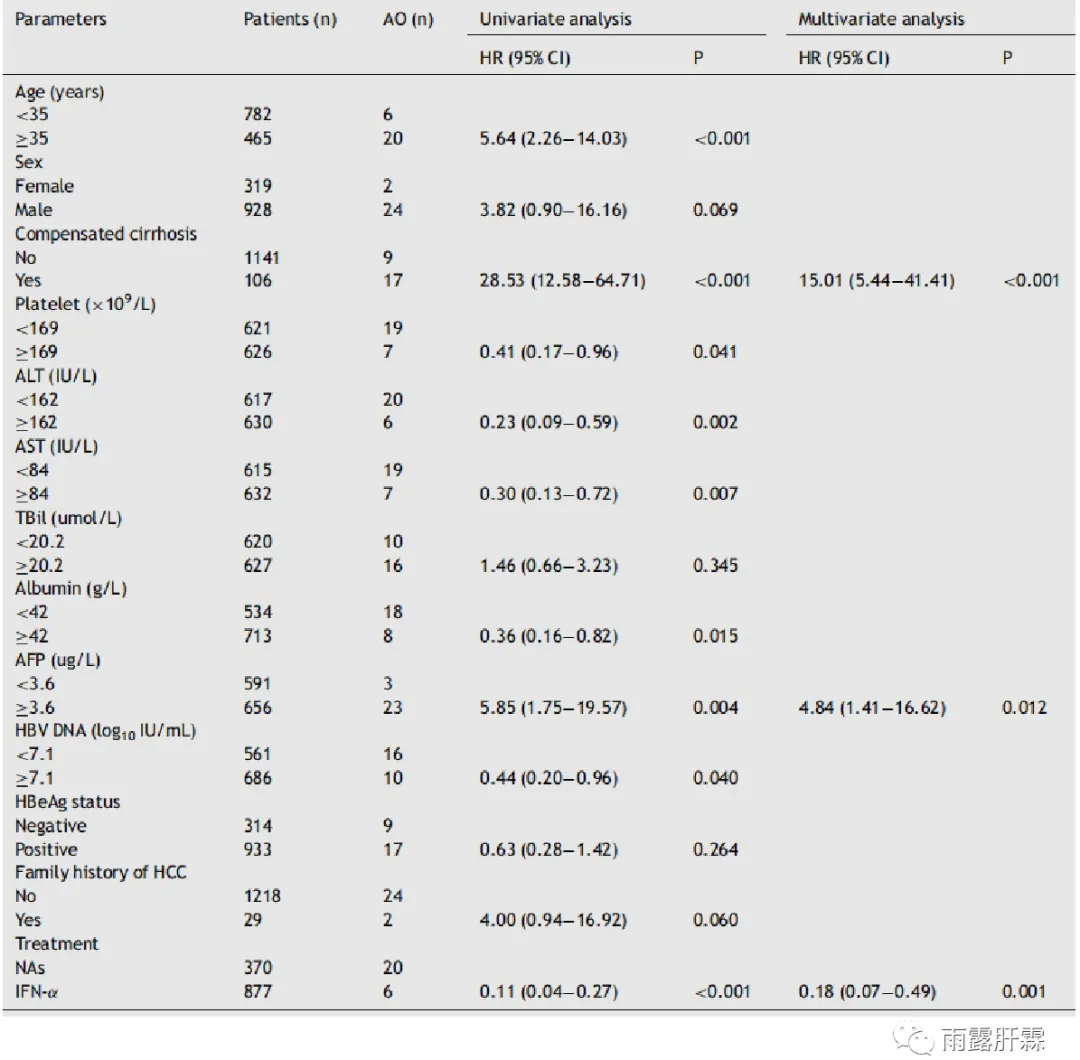
PSM前,多因素分析发现基于IFNα治疗是不良结局发生的唯一独立相关保护因素(HR=0.18;95%CI:0.07-0.49;P=0.001),而代偿期肝硬化和AFP≥3.6μg/L是独立相关危险因素。
全队列中与不良结局相关因素的单因素和多因素分析
图片
PSM后,IFNα治疗仍然是不良结局发生的唯一独立相关保护因素(HR=0.03;95%CI:0.00-0.26;P=0.002),而代偿期肝硬化是唯一独立相关危险因素(HR=43.91;95%CI:7.71-250.13;P<0.001)。
全队列PSM后与不良结局发生相关的独立因素
03 初治队列PSM前后,IFNα组的不良结局发生风险均显著低于NAs组
NAs组和IFNα组分别有20例和5例患者发生不良结局。IFNα组的累积不良结局发生率显著低于NAs组(2.2%vs.14.5%,P<0.001)。不论是对于非肝硬化和肝硬化患者,IFNα组的累积不良结局发生风险均显著低于NAs组(P=0.002,P=0.013)。
PSM后,IFNα组的累积不良结局发生率仍然显著低于NAs组(3.9%vs.12.4%,P=0.002)。
 初治队列IFNα组和NAs组PSM前后的累积不良结局发生率
初治队列IFNα组和NAs组PSM前后的累积不良结局发生率
04 对于肝癌高风险的慢乙肝患者,IFNα治疗降低肝癌发生风险显著优于NAs
通过多个HBV相关肝癌风险预测模型将患者分为高低风险组,对于肝癌高风险的慢乙肝患者(CU-HCC≥5,REACH-B≥8,PAGE-B≥10,或AGED≥5),IFNα组的累积肝癌发生风险均显著低于NAs组(分别为1.6%vs.12.8%,P<0.001;1.2%vs.10.8%,P<0.001;1.6%vs.13.4%,P<0.001;1.2%vs.10.7%,P<0.001)。但对于肝癌低风险组,两组无显著差异。
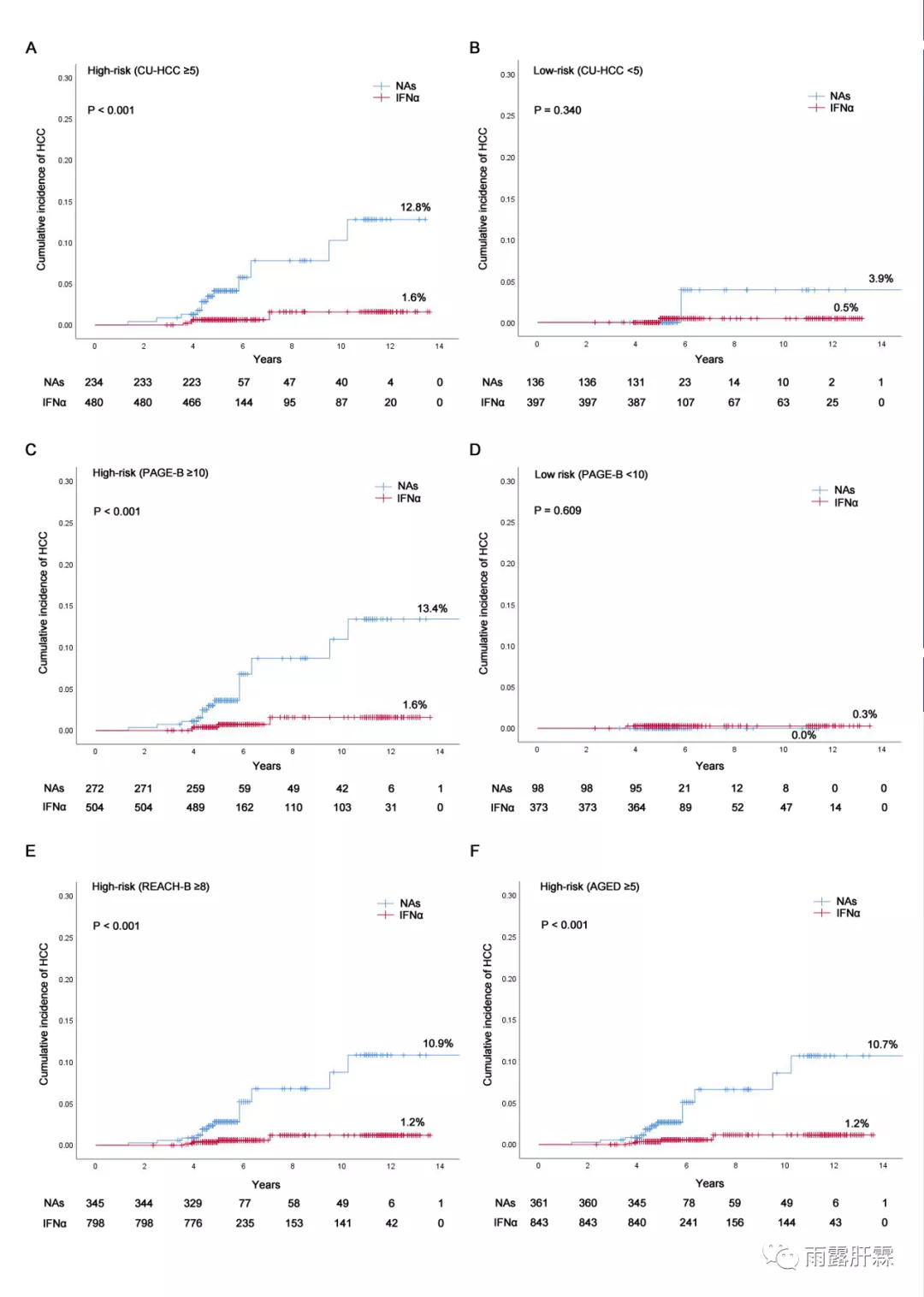 根据肝癌风险分层模型分层分析不同组的累积肝癌发生风险
根据肝癌风险分层模型分层分析不同组的累积肝癌发生风险
肝霖君有话说
本研究从大样本量的回顾性数据分析证实基于IFNα的治疗降低慢乙肝患者不良结局发生风险显著优于NAs。本研究的不良结局不仅仅包含了肝癌,还包含了失代偿肝硬化、肝衰竭、肝移植和死亡等多个远期结局。另外,不论患者是否有代偿期肝硬化,基于IFNα治疗的患者的远期不良结局发生风险都显著低于NAs组,这也从侧面说明了即便是有代偿期肝硬化,也可以积极的采用IFNα治疗达到远期更好的获益。
本研究也采用了肝癌风险分层模型对慢乙肝患者的肝癌风险进行分层分析,再次证实了之前研究的结论,对于肝癌高风险人群,IFNα降低肝癌发生风险显著优于NAs。因此慢乙肝患者要积极进行肝癌风险评估,及时进行合理的抗病毒治疗,将远期不良结局风险降至最低。
参考文献:
MaoQG,LiangHQ,YinYL,etal.ComparisonofInterferon-alpha-basedtherapyandnucleos(t)ideanalogsinpreventingadverseoutcomesinpatientswithchronichepatitisB.ClinResHepatolGastroenterol,2021:101758.
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。










全部评论:暂无评论