EASL2021:Arrowhead在研乙肝新药ARO HBV(JNJ-3989)在中度肝损伤研究结果公布
AROHBV(JNJ-3989)是一款由Arrowhead与杨森公司共同开发用于慢性乙型肝炎治疗的在研短RNAi(siRNA)疗法药物,由乙型肝炎病毒特异性、肝靶向N-氨基半乳糖结合的短链干扰核糖核酸(SiRNA)触发器JNJ-73763976和JNJ-73763924组成,它们能沉默宿主整合的HBVDNA和游离DNA的HBVRNA转录本。
在此前的2020年欧洲肝病学会年会上发表的一项研究结果显示,JNJ-73763989皮下注射,每月1次共3次,每次100-400mg+核苷(酸)类似物,能使慢性乙型肝炎患者乙肝表面抗原(HBsAg)下降大于等于1log10IU/mL,39%的患者在停药48周后仍保持着这种降低。(查看详细内容:EASL2020:在研乙肝新药JNJ-3989(AROHBV)9个月随访数据公布)

在近日举办的欧洲肝病学会年会上,研究人员发表了评估JNJ-73763989在非乙型肝炎病毒感染导致的中度肝损害(Child-PughB)参与者中的药代动力学(PK)、安全性/耐受性研究结果,并与肝功能正常的健康参与者进行了比较。
73763989HPB1002(NCT04208386)是一项Phase1期单剂量、开放标记、平行试验。8名Child-PughB级受试者和8名健康受试者在性别、年龄(±10岁)和体重(±10kg)匹配的情况下接受单剂量200mg皮下注射JNJ-73763989。在72小时内收集JNJ-73763976和JNJ-73763924的血浆和尿液浓度,并使用与荧光检测器耦合的液相色谱进行分析。使用非隔室分析(WinNonlin,Certara,PrincetonNJ)评估药代动力学(PK)参数。全程进行安全性/耐受性评估。
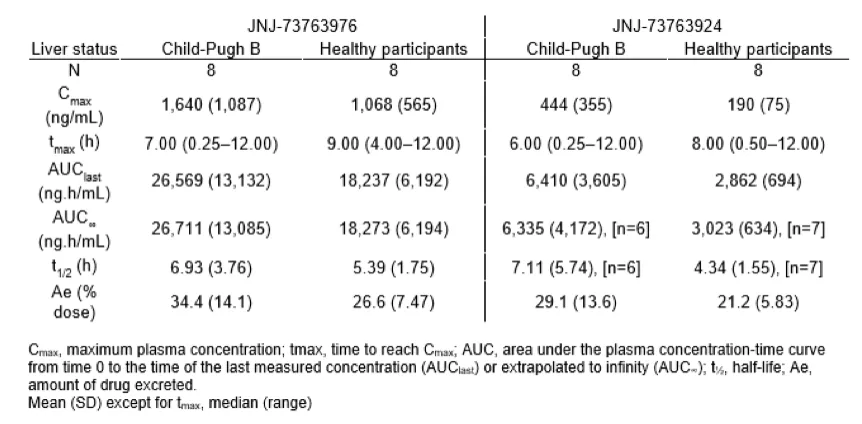
主键参数汇总(表)。在Child-PughB级参与者中,JNJ-73763976的Cmax和AUC值的几何平均比分别高于对照组受试者1.4倍和1.3倍;JNJ-73763924的Cmax和AUC值分别高2.2倍和2.0倍。在Child-PughB级参与者中,两种分析物的半衰期和肾排泄量都略高。
研究过程中没有死亡、严重不良事件(AEs)或停药发生。总体而言,2名参与者(每组各1名)报告了≥1级治疗中出现的不良事件(TEAE)。TEAE为轻/中度,与JNJ-73763989用药无关。除2名Child-PughB级受试者出现一过性血小板从筛查时的2级降至3级外,所有治疗中出现的分级实验室异常均为轻/中度。没有相关的心血管疾病发现。
综上,研究发现,中度肝损伤的受试者暴露于JNJ-73763976和JNJ-73763924的几率较高。单剂200mg的JNJ-73763989在无/有中度肝损伤的参与者中耐受性良好。(更多肝病新药研究信息敬请关注“肝脏时间”微信公众号)!
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。










全部评论:暂无评论