EASL2021:在研乙肝新药siRNA疗法VIR-2218 II期临床最终数据公布
VIR-2218是一种正在研究的N-乙酰半乳糖胺(GalNAc)偶联小干扰核糖核酸(siRNA)疗法药物,采用增强稳定化学加(ESC+)化学方法制成,此方法既保持了增强体内效力所需的代谢稳定性,同时还减少了序列匹配的脱靶效应。VIR-2218靶向乙型肝炎病毒(HBV)保守的X区域,设计用于沉默所有10种HBV基因型的所有HBV转录本,包括cccDNA和整合DNA。
在此前的公开场合已有部分Phase2期临床试验数据相继公布(详情可在肝脏时间微信公众号历史文章中查找)。在本届欧洲肝病学会年会上,研究人员公布了该款药物在慢乙肝患者中进行的Phase2期临床的最终安全性和抗病毒活性数据。

研究纳入了接受核苷酸逆转录酶抑制剂治疗且无明显纤维化/肝硬化的HBeAg阳性或HBeAg阴性病毒抑制慢乙肝患者作为受试对象,在第1天(第0周)和第29天(第4周)接受了2剂量的VIR-2218皮下注射或安慰剂治疗。
四个队列HBeAg阴性受试者分别接受20mg、50mg、100mg或200mg的VIR-2218用药;两个队列的HBeAg阳性受试者接受50mg或200mg;包含4名或8名受试者的队列按3:1的比例随机分配接受VIR-2218或安慰剂治疗。
评估包括安全性和HBsAg水平和其他病毒标志物,所有受试对象在第二剂用药后进行为期12周的随访,对达到预定HBsAg下降目标的患者进行额外32周的随访观察。
24名慢性乙肝型肝炎患者接受了VIR-2218(18HBeAg-;6HBeAg+)用药治疗。接受20mg、50mg、100mg和200mgVIR-2218的HBeAg阴性参与者的最大平均HBsAglog10IU/mL下降分别为1.03、1.23、1.50和1.65。接受50mg和200mgVIR-2218的HBeAg阳性参与者,HBsAglog10IU/mL的最大平均下降幅度分别为1.16和1.57。
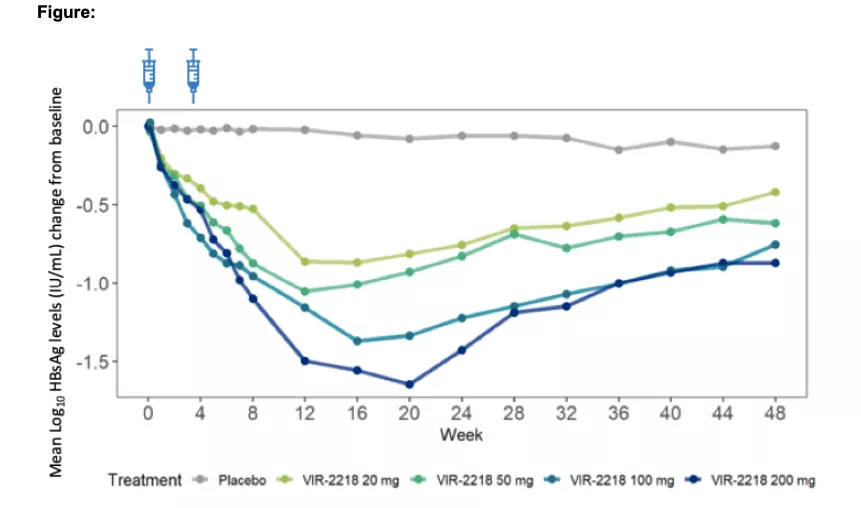
大多数参与者在第16周达到最大HBsAg下降。大多数参与者的HBVDNA和HBVRNA水平在基线时低于最低检测下限,并且未检测到显著变化。
在接受200mgVIR-2218的HBeAg阳性受试者中观察到qHBeAg和HBcrAg下降。
没有参与者因不良事件(AE)而中断,并且大多数治疗中出现的AE严重程度较轻。没有观察到临床上显着的ALT升高。
综上数据,研究认为,在参与此次研究的慢乙肝患者中,两剂20-200mg的VIR-2218间隔4周用药的耐受性良好。在所有剂量水平的HBeAg阴性和HBeAg阳性参与者中都观察到HBsAg显著降低,这表明VIR-2218可能会沉默来自cccDNA和整合DNA的转录本。该项研究中证明的VIR-2218的抗病毒活性支持将其作为针对功能性治愈的联合方案的一部分进行继续开发。(更多肝病新药研究信息敬请关注“肝脏时间”微信公众号)!
注:转载原创文章请务必注明“来源:肝脏时间(HeparSpace)微信公众号”,否则小心作者追到你家门口(⊙o⊙)哦!
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。











全部评论:暂无评论